A ideia desse tipo de documento, elaborado pelo American College of Cardiology, é de publicar novas evidências — mesmo que ainda não tenham sido incorporadas às diretrizes — sobre determinado assunto. Reconhecendo a urgência da avaliação e manejo do Choque Cardiogênico (CC), o ACC reuniu, então, um grupo de especialistas internacionais em uma mesa-redonda virtual, composta por profissionais de diversas especialidades, para abordar questões críticas não resolvidas sobre o CC.
O choque cardiogênico é uma síndrome complexa, heterogênea e multifatorial, na qual a disfunção cardíaca leva a um débito cardíaco insuficiente, resultando em hipoperfusão de órgãos-alvo. A importância do tema é que a mortalidade a curto prazo varia entre 30% e 40%, e a mortalidade em um ano pode atingir ou superar 50%.
O CC secundário ao infarto agudo do miocárdio (IAM-CC) é a forma mais estudada dessa síndrome em ensaios clínicos randomizados. No entanto, a incidência e a prevalência do CC associado a causas não relacionadas ao IAM, especialmente o choque cardiogênico associado à insuficiência cardíaca (IC-CC), aumentaram na última década.
Essas formas diferem em características basais, comorbidades, utilização de recursos e desfechos hospitalares. Apesar dos avanços na revascularização e do uso crescente de suporte circulatório mecânico temporário (tMCS) nas últimas duas décadas, os ensaios clínicos randomizados não conseguiram identificar estratégias terapêuticas que reduzam de forma consistente a mortalidade, exceto a revascularização precoce no IAM-CC.
Definições importantes
- Choque Cardiogênico (CC): Distúrbio cardíaco que resulta em evidências clínicas e bioquímicas de hipoperfusão tecidual sustentada, independentemente da pressão arterial subjacente.
- IAM-CC: CC secundário ao IAM, independentemente da presença ou ausência de supradesnivelamento do segmento ST. O CC decorrente de bradiarritmias, taquiarritmias, bloqueio cardíaco avançado, parada cardíaca ou outras complicações do IAM também é classificado como IAM-CC.
- IC-CC: CC causado por disfunção miocárdica primária, atribuída a etiologias isquêmicas ou não isquêmicas da cardiomiopatia.
Avaliação inicial
Tradicionalmente, os critérios utilizados para diagnosticar CC incluem hipotensão e hipoperfusão de órgãos-alvo, além de evidências de congestão ou redução do débito cardíaco. No entanto, esses critérios simplificam excessivamente uma condição dinâmica e não reconhecem as consequências adversas do CC normotenso, que está associado a um aumento da mortalidade.
O diagnóstico de CC começa com a suspeita clínica de um estado subjacente de débito cardíaco inadequado em pacientes de risco. Essa suspeita pode ser confirmada com dados clínicos, laboratoriais e/ou de imagem.
Os seguintes elementos são fundamentais para o diagnóstico inicial de CC:
- Sintomas
- Exame físico
- Sinais vitais
Achados que aumentam a suspeita de CC:
- Hipotensão
- Alterações da frequência cardíaca e perfusão
- Alterações na perfusão tecidual
- Evidências de congestão e hipoperfusão
Confirmação laboratorial
A suspeita clínica deve ser complementada com exames laboratoriais, incluindo:
- Função renal e hepática
- Gasometria arterial ou venosa
- Lactato venoso ou arterial > 2 mmol/L
- Sódio sérico
- Troponina e pró-BNP
- Cateter venoso central (se disponível) para medir pressão venosa central e saturação venosa central de oxigênio
Exames complementares essenciais
Eletrocardiograma: avaliar sinais de isquemia miocárdica aguda. Se houver supradesnivelamento do segmento ST, o paciente deve ser rapidamente encaminhado para cateterismo cardíaco.
Ecocardiograma transtorácico ou ultrassom cardíaco à beira do leito para identificar:
- Disfunção ventricular esquerda (VE) ou direita (VD)
- Tamponamento cardíaco
- Valvopatias agudas
Mnemônico para Diagnóstico Rápido de CC: SUSPECT CS
(S – sinais/sintomas, U – urinário (débito), S – sustentada hipotensão, P – perfusão, E – ECG e ECOTT, C – congestão, T – triagem)
| Categoria | Achados Clínicos e Laboratoriais |
| Sintomas/Sinais | Alteração do estado mental, confusão, dor torácica ou pressão no peito, extremidades frias e úmidas pulso rápido, pressão de pulso baixa (< 25% da PAS), pressão venosa jugular elevada, estertores, ortopneia, dispneia paroxistica noturna, edema de membros inferiores. |
| Débito urinário | Oligúria ou anúria. < 30 mL/h (< 0,5 mL/kg/h). |
| Hipotensão sustentada | PAS < 90 mmHg, PAM < 65 mmHg por > 30 min. queda > 30 mmHg da pressão basal, ou necessidade de suporte farmacológico/mecânico para manter PAS > 90 mmHg. |
| Perfusão | Marcadores de hipoperfusão: lactato > 2 mmol/L, ALT > 200 U/L ou 3x o limite superior da normalidade, creatinina 2x a limite superior da normalidade, pH < 7,2, acidose metabólica sem outra causa conhecida. |
| ECG/Ecocardiograma | Avaliação de isquemia aguda, incluindo evidência eletrocardiográfica e ecocardiográfica de IAM com supra de ST (alterações regionais da motilidade ventricular); dilatação e disfunção sistólica do VE ou VD: valvopatias. |
| Congestão | Presença ou ausência de congestão com base nos achados clínicos e hemodinámicos identificação do ventriculo envolvido (VE vs VD vs Biventricular). |
| Triagem | Ativação da equipe de choque cardiogênico ou consideração de transferência para nível de cuidado mais avançado. |
Importante destacar que a suspeita inicial e o diagnóstico de choque cardiogênico (CC) não requerem hemodinâmica invasiva. No entanto, essa avaliação é frequentemente útil para esclarecer o envolvimento ventricular e o perfil congestivo do paciente.
Uma vez feito o diagnóstico, a gravidade do CS deve ser classificada usando o famoso sistema de estadiamento da SCAI.
Transferência para centros especializados
O documento recomenda que os hospitais de Nível 2 e 3 (hospitais regionais) identifiquem:
- Os recursos locais disponíveis para manejo do CS.
- Um centro especializado em CC que possa aceitar transferências para avaliação e tratamento adicionais, além de oferecer consultoria remota para pacientes que não são candidatos à transferência imediata ou que precisam de estabilização antes da transferência.
Pacientes que devem ser imediatamente transferidos para centro especializado em choque cardiogênico:
- Parada cardíaca com status neurológico incerto.
- Uso de ≥ 1 droga vasoativa.
- Indicação de tMCS
Avaliação hemodinâmica invasiva
Dados observacionais sugerem que a avaliação hemodinâmica invasiva é útil para caracterizar o fenótipo do CC, avaliar a gravidade do choque e orientar decisões sobre escalonamento e retirada do suporte circulatório mecânico temporário.
A hipótese científica de que a avaliação hemodinâmica invasiva precoce (dentro de 6 horas da randomização) reduz a mortalidade está atualmente sendo testada no estudo PACCS (Pulmonary Artery Catheter in Cardiogenic Shock) em pacientes com CC-IC.
Perfis hemodinâmicos no CC
- Congestão VE dominante:
Caracterizada por pressão capilar pulmonar elevada ou pressão diastólica final do VE > 15 mmHg.
- Congestão VD dominante:
Pressão capilar pulmonar normal com pressão atrial direita (PAD) elevada (PAD > 15 mmHg).
- Congestão biventricular:
Elevação simultânea das pressões atrial direita e capilar pulmonar.
Associada a piores desfechos, incluindo mortalidade, necessidade de LVAD e transplante cardíaco.
A comissão recomenda associar a avaliação hemodinâmica invasiva com imagem cardíaca não invasiva (ecocardiografia ou ultrassonografia point-of-care) sempre que disponível.
Manejo farmacológico
O objetivo deve ser aliviar a congestão, otimizar o débito cardíaco e melhorar a perfusão dos órgãos vitais.
Sempre que existir um fenótipo congestivo, ele deve ser tratado com diuréticos de alça intravenosos, associação com diuréticos tiazídicos e terapia de substituição renal caso a congestão seja refratária.
A hipoperfusão pode ser tratada iniciando-se medicações vasoativas intravenosas, incluindo inotrópicos, cronotrópicos, inopressores, inodilatadores, vasodilatadores e vasopressores.
O comitê destaca que os medicamentos vasoativos devem ser usados na menor dose possível para garantir a perfusão adequada e pela menor duração possível.
Uma análise Cochrane encontrou evidências insuficientes para apoiar a superioridade de um inotrópico ou agente vasodilatador específico na CS, especialmente em relação ao benefício em mortalidade.
O documento faz algumas considerações sobre o tratamento farmacológico:
- Inodilatadores ou vasodilatadores podem ser considerados em CC com pressão normal, especialmente em pacientes com aumento da resistência vascular sistêmica. A milrinona, devido à sua meia-vida relativamente longa e excreção renal, deve ser usada com cautela em pacientes com função renal piorando.
- Cronotrópicos podem ser testados no CC induzido por bradicardia.
- Embora não haja consenso claro sobre a escolha do agente vasoativo de primeira linha, o comitê coloca a norepinefrina como escolha razoável para a maioria dos pacientes.
Suporte mecânico
Os ensaios clínicos randomizados sobre o uso de tMCS na CS têm se concentrado principalmente na CS associada a IAMCST e têm sido limitados por tamanho de amostra, desenho do estudo, seleção de pacientes, tempo e outras limitações importantes.
Embora o uso de tMCS esteja sendo cada vez mais empregado no tratamento tanto de CC-IAM quanto de CC-IC, o uso rotineiro de tMCS em todos os pacientes com CS é fortemente desaconselhado.
O estudo “Intraaortic Balloon Pump in Cardiogenic Shock (IABPSHOCK) II” foi um ensaio randomizado com 600 pacientes com IAM-CC que não demonstrou efeito na mortalidade geral em 30 dias e no acompanhamento de longo prazo de 6 anos.
O estudo “Extracorporeal Life Support in Infarct-Related Cardiogenic Shock (ECLS-SHOCK)” foi um ensaio randomizado com 420 pacientes com IAM-CC para os quais se planejou revascularização precoce, e mostrou que a mortalidade geral em 30 dias não foi menor entre os pacientes que receberam suporte extracorpóreo precoce.
De fato, o estudo “DanGer Shock” foi o primeiro a demonstrar que o uso precoce do Impella CP em pacientes selecionados com choque relacionado ao IAMCST melhorou a sobrevida em 180 dias em comparação com o padrão de cuidado, com uma redução absoluta da mortalidade de 12,7%.
Do ponto de vista mecânico, o objetivo do tMCS é promover o descarregamento ventricular, além de restaurar a perfusão sistêmica, sendo projetado para fazer a ponte do paciente com CS para terapias avançadas ou facilitar a recuperação miocárdica.
Além disso, o uso de tMCS pode permitir a desescalada e a redução das terapias farmacológicas que podem exacerbar danos ou isquemia miocárdica se continuadas em altas doses por longo período. Os princípios subjacentes à adição ou escalada do tMCS devem ser baseados no índice cardíaco desejado para melhorar a perfusão quando o suporte farmacológico sozinho for inadequado 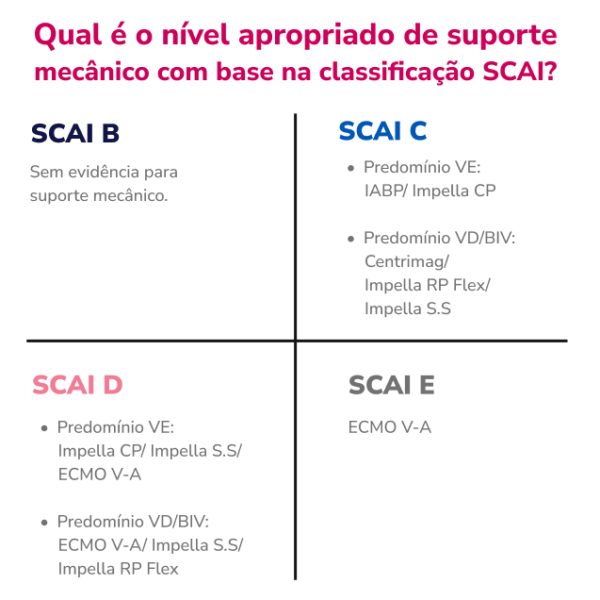
No caso específico de CC-IC, o balão intraaórtico pode ser considerado no SCAI B.
Complicações e manejo do suporte circulatório mecânico
Complicações do acesso vascular de grande calibre incluem sangramento e isquemia de membros, sendo necessárias monitorização rigorosa e intervenções preventivas.
No IAM-CC, o sangramento grave pode ocorrer em até 60% dos casos, e o risco de isquemia de membros é quatro vezes maior em pacientes que necessitam de tMCS.
Estratégias para reduzir essas complicações incluem minimizar a duração do acesso vascular e remover dispositivos de grande calibre (> 12 French) em ambiente controlado, como sala de hemodinâmica ou centro cirúrgico, sempre que possível.
Se ocorrer sangramento incontrolável ou isquemia de membros, a remoção imediata do dispositivo tMCS é geralmente necessária.
Desmame do tMCS
O desmame deve ser feito de forma progressiva, reduzindo o fluxo do dispositivo de maneira escalonada, ajustando-se conforme a reversibilidade da lesão cardiovascular inicial. Em geral, a redução do suporte ocorre a cada 2 a 4 horas em incrementos de 0,5 a 1 L/min (equivalente a redução de 2 níveis de desempenho no Impella). Pacientes com CS devido à insuficiência cardíaca aguda sobreposta à crônica podem necessitar de uma transição com suporte inotrópico prolongado.
Ventilação mecânica
O documento destaca que a pressão expiratória positiva final (PEEP) pode aumentar a resistência vascular pulmonar, reduzir pré-carga do VE e VD, diminuir pós-carga do VE e alterar a complacência ventricular pelo efeito da interdependência ventricular.
Para pacientes com falência do VE, com ou sem insuficiência mitral grave, a ventilação com pressão positiva pode ser benéfica ao reduzir a pós-carga e melhorar o volume sistólico.
Se houver falência principalmente de VD, a intubação deve ser realizada apenas se extremamente necessária. Deve-se usar a menor peep possível para atingir saturação > 92%.
Conclusão
O choque cardiogênico continua sendo uma síndrome complexa, com alta morbidade e mortalidade. O reconhecimento precoce e a estratificação de risco são fundamentais para iniciar rapidamente o suporte farmacológico e/ou tMCS. A monitorização hemodinâmica invasiva pode ser útil para guiar a escolha e escalonamento da terapia. A reavaliação seriada, especialmente nas primeiras 24 horas, é essencial para garantir estabilidade hemodinâmica, restaurar a perfusão tecidual e minimizar lesões de órgãos-alvo.
Quer acompanhar esse e outros temas importantes da área da cardiologia? Acompanhe a cobertura completa do ACC 25 com a Afya, de modo online e gratuito, e se atualize nos principais assuntos da área. Inscreva-se aqui!
Autoria

Juliana Avelar
Médica formada pela Universidade Federal Fluminense (UFF). Cardiologista pelo Instituto Dante Pazzanese de Cardiologia
Como você avalia este conteúdo?
Sua opinião ajudará outros médicos a encontrar conteúdos mais relevantes.

