A tecnologia vem cada vez mais se tornando parte fundamental no tratamento do diabetes mellitus tipo 1 (DM1). Nos últimos anos, vimos uma evolução gigantesca em termos tecnológicos quanto aos sistemas de infusão contínuos de insulina (SICI), também conhecidas como “bombas de insulina”.
Mais recentemente, novos trials tem demonstrado o impacto em controle glicêmico de dispositivos em alça fechada, capazes de controlar a taxa de infusão basal de insulina após a leitura da glicose intersticial realizada por um monitor contínuo de glicose (CGM) acoplado ao sistema. Sistemas como a OMNIPod 5 (insulet) ou a minimed 780g da Medtronic vem demonstrando sua capacidade de aumentar significativamente o tempo no alvo (time in range, 70-180 mg/dL) de pacientes em uso desses dispositivos mesmo quando comparados aos SICIs mais antigos/convencionais, sem sistema de controle em alça fechada.
Para introduzir melhor o assunto, vale a pena uma breve revisão acerca dos diferentes tipos de dispositivos de infusão de insulina disponíveis.
Basicamente, podemos dividir as “bombas” de insulina em quatro grandes grupos:
1) Sistemas de Infusão Contínua de Insulina (SICI): São as “Bombas” de insulina convencionais, onde é necessário a programação manual da dose basal (utilizando insulina de ação rápida) e cálculo de bolus, com necessidade de ajustes pelo endocrinologista nas consultas de acordo com o perfil glicêmico. Nesse tipo de dispositivo é possível ajustar basais temporários e adicionar eventos de saúde para diferenciação de doses basais nesses momentos. Um exemplo é a Accu-chek spirit Combo.
2) Bombas com sensibilidade aumentada: Também conhecidas como “alça fechada parcial”, apesar de não conseguirem realizar ajustes automáticos na taxa de infusão, são capazes de suspender a infusão de insulina se predição de queda, com objetivo de reduzir o risco de hipoglicemias. Para isso, já se torna um dispositivo mais complexo e com necessidade de se acompanhar do uso de um CGM. É composta por 3 Partes: Bomba, CGM e algoritmo que suspende automaticamente a infusão de insulina caso haja predição de hipoglicemia nos próximos 30 minutos, de acordo com a tendência da glicose vista no CGM. Um exemplo é a MiniMed 640G, da Medtronic.
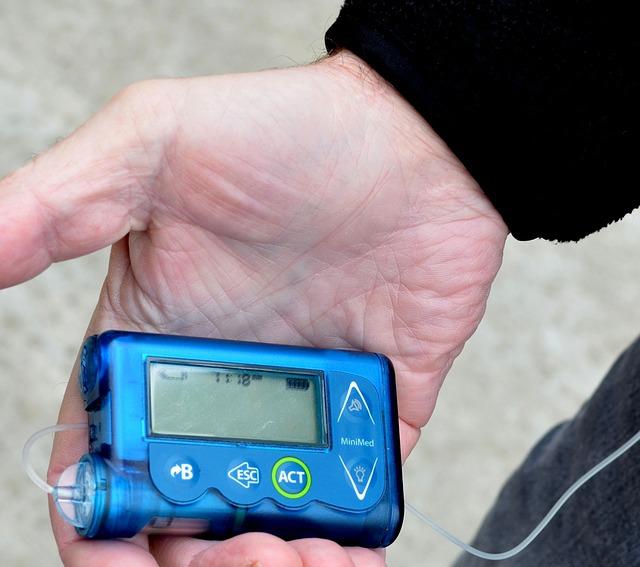
3) Entrega automatizada de insulina: Estes são os dispositivos “closed loop” (alça fechada), conhecidos nos artigos em inglês como Automated Insulin Delivery (AID). Tais dispositivos são capazes de ajustar a taxa de infusão de insulina basal conforme a glicose checada pelo CGM, com capacidade tanto de redução na dose como de aumento para corrigir períodos de hiperglicemia. Tais dispositivos requerem apenas a programação do bolus. São exemplos a MiniMed 780G (Medtronic) e a OmniPod 5.0 (Insulet). É sobre um modelo dessa categoria que vamos discutir a respeito neste artigo.
4) Pâncreas biônico: Por fim, a forma mais sofisticada de entrega de insulina é através do pâncreas artificial/biônico, que é capaz de sozinho realizar o ajuste e programação da dose de insulina basal e bolus. Temos apenas um representante nessa categora, a iLet (BetaBionics), cujo estudo foi publicado em 2022 no New England Journal of Medicine.
Quanto ao tratamento do DM1, também é sabido que quanto melhor o controle logo ao diagnóstico e nos primeiros anos de tratamento, melhores são os desfechos a longo prazo. Além disso, um dos objetivos atuais no estudo dessa condição é compreender formas de tratamento capazes de preservar a função resquicial de células beta, uma vez que a persistência prolongada do peptídeo C (indicando produção residual de insulina) pode ser benéfica ao melhorar o controle glicêmico e estar associada a menor incidência de complicações microvasculares ao longo dos anos.
Unindo esses dois mundos de pesquisa, foi publicado um ensaio clínico randomizado no Diabetes Care recentemente que analisou o impacto do uso de um sistema em alça fechada no controle e na secreção residual de peptídeo C em indivíduos com DM1 recém diagnosticados.
Leia mais: Diabetes e infecções: o que precisamos saber
O ESTUDO
O estudo, que fez parte do CLOuD Consortium, foi um ensaio clínico randomizado, open label, e foi composto pelo follow-up após um período inicial de 24 semanas, já publicado. O estudo atual totalizou 48 semanas de seguimento.
Os participantes foram randomizados inicialmente (na semana zero) para o uso de um dispositivo automático de insulina (em “alça fechada” – AID – na sigla em inglês) ou tratamento convencional (utilizando múltiplas aplicações diárias – MDI – ou sistemas de infusão contínua convencionais). Praticamente todos os participantes do estudo utilizaram CGM.
Os critérios de inclusão foram indivíduos jovens (entre 10 e 16,9 anos) com DM1 recém diagnosticado (até 21 dias do diagnóstico). Foram excluídos participantes com outras doenças concomitantes ou tratamentos que tivessem potencial de afetar o controle glicêmico ou a interpretação da HbA1c. Todos foram questionados a respeito da vontade de persistir nesse estudo de follow-up após a fase inicial de 24 semanas.
O objetivo primário do estudo foi avaliar o impacto do uso do AID na secreção residual de peptídeo C e no controle glicêmico. As análises foram realizadas em intention-to-treat.
O estudo original, de 24 semanas, contou com 97 participantes. Após as 24 semanas iniciais, 81 participantes (47 no grupo AID e 34 no grupo controle) compuseram o estudo que vamos discutir, sendo que 16 deixaram o estudo e não participaram da presente avaliação.
Quanto à população do estudo, a média de idade foi de 14 anos, cerca de 42 do sexo feminino, com HbA1c inicial de 7,3%.
O dispositivo utilizou o algoritmo de modelo preditivo Cambridge em dois hardwares diferentes, nas configurações FlorenceM e CamAPS FX (todos utilizaram esta configuração entre 36 e 48 semanas)
O uso precoce de bomba closed loop melhorou o controle glicêmico
O uso precoce de bomba closed loop (grupo AID) melhorou o controle glicêmico comparado ao grupo terapia padrão:
- HbA1c: 7,1% vs. 7,9% (dif média -0,9%; IC 95%; -0,2 a -1,5; p = 0,001)
- Tempo no alvo (70 – 180 mg/dL): 12% maior no grupo AID (IC 95%; 3-20%; p = 0,008)
- Tempo acima do alvo (> 180 mg/dL): 10=2% maior no grupo controle (IC 95%; -3 a -21%; p = 0,008)
No grupo AID, 59% atingiram o alvo de HbA1c < 7%, comparado a apenas 22% no grupo padrão. Não foram observadas diferenças quanto ao tempo em hipoglicemia.
Tais benefícios já haviam sido reportados no estudo até 24 semanas, mas o interessante é a manutenção do bom controle por 4 anos após o diagnóstico naqueles que permaneceram em uso dos AID.
Saiba mais: Baricitinibe pode retardar início da terapia com insulina na diabetes tipo 1?
Apesar da melhora glicêmica, não houve diferenças quanto a dosagem do peptídeo C
Apesar da melhora glicêmica, não houve diferenças quanto à dosagem do peptídeo C corrigido para glicemia, demonstrando dessa forma que não houve portanto preservação adicional de células beta (diferença média: -2,0 pmol/mol; IC 95%; -7 a 4; p = 0,54) com o uso do dispositivo mesmo após um período mais prolongado, de 48 semanas.
Outros pontos importantes
A ocorrência de eventos de hipoglicemia grave foram incomuns em ambos os grupos, totalizando apenas 11 eventos ao todo, sendo 6 no grupo AID e 5 no grupo controle, sem diferenças significativas. Além disso, a ocorrência de cetoacidose diabética também foi idêntica em ambos os grupos (3 no grupo AID e 4 no grupo controle).
Perspectivas
O uso de bombas closed loop parece trazer um impacto positivo tanto no controle glicêmico como no conforto e qualidade de vida de indivíduos com DM1, mesmo os recém diagnosticados, porém sem efeitos na preservação de células beta pancreáticas. O guideline da American Diabetes Association (ADA) já recomenda o uso de dispositivos de infusão contínua a todos indivíduos com DM1, preferencialmente AID, sendo que há dados cada vez mais robustos apontando para benefícios reais em termos de controle glicêmico e melhora de tempo no alvo. Os autores do estudo discutido argumentam inclusive o mesmo ponto de vista, de que os AID devem ser oferecidos sobretudo a crianças e jovens desde o momento do diagnóstico do DM1, visto seus benefícios no controle e possível impacto que isso pode trazer a longo prazo.
Por outro lado, é fundamental que os próximos estudos sobre o tema também abordem populações mais diversas, além de estudos de custo efetividade e que políticas públicas sejam consideradas para aumentar a disponibilidade dessas ferramentas que, apesar de boas, atualmente são muito restritas do ponto de vista sócio-econômico.
Autoria

Luiz Fernando Fonseca Vieira
Endocrinologista pelo HCFMUSP ⦁ Telemedicina no Hospital Israelita Albert Einstein (HIAE) ⦁ Residência médica em Clínica médica pela Faculdade de Medicina da Universidade de São Paulo (FMUSP) ⦁ Graduação em Medicina pela Universidade Estadual Paulista Júlio de Mesquita Filho (UNESP) - Faculdade de Medicina de Botucatu
Como você avalia este conteúdo?
Sua opinião ajudará outros médicos a encontrar conteúdos mais relevantes.

