A icterícia neonatal é uma manifestação clínica da elevação da bilirrubina sérica total (BT) que resulta da deposição de bilirrubina na pele e tecidos do bebê recém-nascido (RN). Apresenta-se clinicamente como uma coloração amarelada da pele, esclera e membranas mucosas. A icterícia neonatal corresponde à condição clínica mais frequente e causa comum de reinternação hospitalar após o nascimento: cerca de 60% dos RN a termo e 80% dos prematuros desenvolvem icterícia na primeira semana de vida (1-3).
Os dois tipos de hiperbilirrubinemia neonatal são a não conjugada (HNC) e a conjugada (HC) (3). A HNC é definida como bilirrubina indireta (BI) na concentração igual ou superior a 2 mg/dL. Considera-se HC se a bilirrubina direta (BD) é maior que 1 mg/dL (2).
Na maior parte das vezes, a icterícia espelha uma adaptação fisiológica do metabolismo da bilirrubina durante a transição da vida fetal para a neonatal. Algumas vezes, porém, decorre de um processo patológico (2). Embora seja comum e geralmente benigna, a icterícia neonatal exige atenção especial porque pode evoluir para formas graves de hiperbilirrubinemia, com risco de encefalopatia aguda e sequelas neurológicas permanentes, como kernicterus (4). Isso ocorre porque o cérebro do RN é particularmente vulnerável à toxicidade da BI, que pode atravessar a barreira hematoencefálica (BHE) e causar dano irreversível (5). A icterícia neonatal extrema, associada ao risco de kernicterus, tem uma incidência mundial estimada em 99/100.000 ou mais, afetando 130.000 ou mais RN anualmente, o que exige maior vigilância e preparo para intervenção terapêutica rápida (6).
Metabolismo da bilirrubina
No RN, a bilirrubina é produzida principalmente a partir da degradação das hemácias. Com a destruição dos glóbulos vermelhos, a hemoglobina sofre um catabolismo em duas etapas no sistema retículo-endotelial, resultando na formação de BI (também conhecida como bilirrubina não conjugada). A BI é transportada na circulação ligada à albumina sérica. Ao chegar no fígado, a BI se combina com o ácido glicurônico no retículo endoplasmático liso, originando mono ou diglicuronídeos de bilirrubina hidrossolúveis, conhecidos como BD, também chamada de bilirrubina conjugada (1).
A BD é um componente da bile. Através do sistema biliar, a BD alcança o trato gastrointestinal. Embora uma parcela da BD possa ser hidrolisada pela beta-glicuronidase em BI no intestino delgado, a partir de onde pode ser reabsorvida, caracterizando a circulação entero-hepática, a maior parte é eliminada pelas fezes (1).
O estabelecimento da motilidade intestinal e de um padrão normal de evacuação constitui um componente relevante para reduzir a carga de bilirrubina decorrente da circulação entero-hepática nos primeiros dias de vida. Isso explica, em parte, por que o apoio ao aleitamento materno é um elemento fundamental no manejo da icterícia neonatal (1).
Icterícia fisiológica e patológica: entenda as diferenças
A icterícia neonatal geralmente é uma condição leve, transitória e autolimitada, conhecida como fisiológica. A icterícia fisiológica corresponde a aproximadamente 75% dos casos de hiperbilirrubinemia neonatal e tem origem a partir de uma alteração fisiológica do metabolismo da bilirrubina no período neonatal. No RN, os níveis normais de BT são comparativamente mais elevados e variam de acordo com a idade pós-natal. Mesmo RN a termo e saudáveis apresentam maior carga de bilirrubina devido à maior massa de hemácias e menor sobrevida dos eritrócitos. Além disso, a depuração metabólica da bilirrubina também é comprometida devido à atividade reduzida da enzima uridina difosfato glicuronosiltransferase (UGT), necessária para a conjugação da bilirrubina. O nível de atividade da UGT no RN corresponde a cerca de 1% do observado em adultos. Por fim, os RN apresentam aumento da circulação entero-hepática, um fator adicional para a elevação da BT (3).
Em geral, a icterícia fisiológica surge em RN a termo após 24 horas de vida, atinge o pico entre 48 e 96 horas e se resolve de forma espontânea em duas a três semanas (3). Os fatores de risco relacionados à maior suscetibilidade de RN em desenvolver icterícia fisiológica são: concentração elevada de hemoglobina; sistemas hepáticos de captação, transporte e conjugação imaturos; menor tempo de vida das hemácias em comparação ao de adultos; aumento dos níveis de beta-glicuronidase no intestino, com liberação de maior quantidade de BI para a circulação entero-hepática (1).
Icterícia patológica: quando suspeitar e como definir
Na icterícia patológica, uma condição clínica subjacente ou um fator de risco leva à hiperbilirrubinemia (7). A HC raramente está associada à neurotoxicidade da BT (8). A HNC patológica o corre nas primeiras 24 horas após o nascimento, quando a BT se encontra acima do percentil 95 nos gráficos de bilirrubina específicos para a idade, ou quando há um aumento igual ou superior a 5 mg/dL/dia ou maior que 0,2 mg/dL/h. A etiologia da HNC pode ser subdividida em três categorias: aumento da produção de bilirrubina, redução da depuração da bilirrubina e causas diversas (3).
Aumento da produção de bilirrubina
Diversas condições patológicas aumentam a produção de bilirrubina no RN e bebês com esse aumento tendem a apresentar, consequentemente, concentrações mais altas, a depender também de sua capacidade de eliminá-la. A etiologia do aumento excessivo da produção de bilirrubina é multifatorial, sendo que uma das mais graves e relativamente comuns é a incompatibilidade sanguínea materno-fetal, na qual um teste de Coombs positivo contribui para maior degradação de eritrócitos e, consequentemente, para o aumento da produção de bilirrubina (9).
Redução da depuração da bilirrubina
A HNC devido à diminuição da depuração da bilirrubina resulta geralmente de defeitos quantitativos ou qualitativos na enzima UGT. Três distúrbios resultantes de uma anormalidade desta enzima são a síndrome de Gilbert e as síndromes de Crigler-Najjar tipos I e II (3).
Causas diversas e fatores de risco: visão prática
Os fatores de risco para icterícia neonatal englobam causas genéticas, maternas, perinatais e neonatais.
- Dentre os Fatores genéticos, podemos citar: síndrome de Alagille, síndrome de Crigler-Najjar, síndrome de Gilbert, β-talassemia, deficiência de glicose-6-fosfato desidrogenase (G6PD), polimorfismo da bilirrubina glucuronosiltransferase, defeitos estruturais dos eritrócitos (incluindo esferocitose hereditária e eliptocitose), deficiência de piruvato quinase e galactosemia.
- Fatores maternos incluem: diabetes, gravidez na adolescência, histórico familiar de icterícia grave, incompatibilidade ABO, incompatibilidade Rh, primiparidade e uso de medicamentos durante o trabalho de parto (incluindo ocitocina, bupivacaína e prometazina). J
- Já os Fatores perinatais: englobam asfixia perinatal, clampeamento tardio do cordão umbilical, via de parto (pélvica vs. cefálica, instrumentação), trauma no momento do parto (cefalohematoma ou hematoma significativo), infecções congênitas (incluindo sífilis e citomegalovírus) e sepse (8).
- Por fim, os Fatores neonatais são: sexo masculino, prematuridade ou baixo peso ao nascer e pequeno para a idade gestacional (PIG), hipoglicemia, hipotermia, hipotireoidismo, policitemia, irmão anterior recebeu fototerapia ou exsanguinotransfusão, concentração de BT ou transcutânea antes da alta hospitalar na zona de alto risco, uso de agentes hemolíticos (como produtos à base de mentol ou naftaleno) em grupos populacionais com deficiência de G6PD, deficiência de folato, aflatoxinas e nascimento fora de um ambiente hospitalar (8).
No RN, a HNC também pode resultar de causas relacionadas à amamentação, sendo a icterícia associada ao aleitamento materno exclusivo particularmente comum. A ingestão insuficiente de leite pode ocasionar hiperbilirrubinemia por ingestão inadequada no início da primeira semana de vida, levando à redução da motilidade intestinal e da excreção de bilirrubina. Por outro lado, a icterícia associada ao leite materno aparece mais tardiamente, atinge o pico na segunda semana e geralmente é benigna, apesar da elevação prolongada (3).
Raça/etnia não deve ser usada para estratificar risco (AAP 2022)
Segundo a Academia Americana de Pediatria (AAP), a raça ou etnia do RN não deve ser usada para avaliar o risco de hiperbilirrubinemia. A diretriz da AAP atualizada em 2022 sobre hiperbilirrubinemia neonatal não incluiu a raça, embora a AAP tenha incluído anteriormente a raça do Leste Asiático como fator de risco para hiperbilirrubinemia grave e a raça negra como fator associado à diminuição do risco (4,10). O uso de categorias raciais para avaliar o risco de hiperbilirrubinemia não tem sido associado à redução das taxas de kernicterus e pode estar associado a danos (3).
Quadro 1 – Etiologia da hiperbilirrubinemia não conjugada
|
|
Com hemólise |
Sem hemólise |
|
Causas frequentes |
Incompatibilidade de grupos sanguíneos: ABO, Rh, Kell, infecção por Duffy |
– Icterícia fisiológica – Icterícia associada ao aleitamento materno – Hemorragia interna – Policitemia – Filho de mãe diabética |
|
Causas raras | – Defeitos enzimáticos dos eritrócitos: deficiência de glicose-6-fosfato desidrogenase, deficiência de piruvato quinase
– Distúrbios da membrana dos eritrócitos: esferocitose, ovalocitose – Hemoglobinopatias: talassemia |
– Mutações da enzima uridina difosfato glicuronosiltransferase (UGT) (síndrome de Crigler–Najjar, doença de Gilbert) – Estenose pilórica – Hipotireoidismo – Trombocitopenia imune |
Fonte: Adaptado de Gowen Jr., 2023 (11).
O que é kernicterus e quais estruturas podem ser afetadas?
A encefalopatia bilirrubínica crônica ou kernicterus consiste no acúmulo de bilirrubina no cérebro, observado durante necrópsias de bebês que faleceram em decorrência de toxicidade aguda pela bilirrubina. O envolvimento do tronco encefálico, hipocampo, cerebelo, globo pálido e núcleos subtalâmicos foi descrito. Essa predisposição anatômica pode estar relacionada ao aumento da atividade metabólica e do fluxo sanguíneo cerebral regional (1).
Definição clínica (AAP) e manifestações: precoces e tardias
Segundo a AAP, o termo “kernicterus” refere-se à condição neurológica incapacitante permanente caracterizada por alguns ou todos os seguintes sintomas: paralisia cerebral coreoatetoide; paresia do olhar para cima; displasia do esmalte dos dentes decíduos; perda auditiva neurossensorial ou neuropatia auditiva ou distúrbio do espectro da dissincronia, e achados característicos em exames de ressonância magnética de crânio (10).
As manifestações clínicas mais precoces incluem hipotonia, letargia, irritabilidade, diminuição do reflexo de Moro, dificuldade para alimentação, choro agudo e vômitos são as manifestações clínicas mais precoces do kernicterus, acionando um alerta. Em geral, esses sinais iniciais costumam ser observados após o quarto dia de vida. Já os sinais tardios englobam fontanela abaulada, convulsões, paralisia do olhar para cima, postura em opistótono, hemorragia pulmonar, febre e hipertonia. Infelizmente, as formas graves podem evoluir para óbito ainda no período neonatal. Em sobreviventes, a espasticidade tende a regredir em sobreviventes, porém podem surgir sequelas permanentes, como surdez neurossensorial, paralisia cerebral coreoatetósica, deficiência intelectual, displasia do esmalte e alteração da coloração dentária (11).
Fatores de risco para kernicterus (prematuros)
Em prematuros, os fatores de risco para kernicterus são: albumina sérica <2,5 g/dL; Apgar < 3 no 5º minuto; peso ao nascer < 1000g; sepse; pressão arterial de oxigênio <40 mmHg por >2 h; pH <7,15 por mais de 1 h; temperatura corpórea <35°C por >4 h; rápido aumento de BT sugerindo doença hemolítica; deterioração clínica – apneia e bradicardia que requer ventilação/intubação ou hipotensão com necessidade de tratamento nas últimas 24h (2). Em RN a termo, os fatores de risco descritos na literatura incluem o nível de BT >340 mmol/litro, aumento rápido do nível de BT (>8,5 mmol/litro/hora) e sinais clínicos sugestivos de encefalopatia bilirrubínica (1). Hipoalbuminemia (albumina sérica <30 g/L), suspeita ou diagnóstico de hemólise, suspeita de sepse ou confirmação por cultura e instabilidade hemodinâmica ou respiratória significativa (ou ambas) nas 24 horas anteriores também são mencionados na literatura (12).
Prevenção e conceitos relacionados (DEK e escore BIND)
A prevenção do kernicterus consiste em evitar níveis excessivamente elevados de BI e a exposição a condições ou medicamentos que deslocam a bilirrubina da albumina. Em alguns casos, os sinais iniciais podem ser revertidos com exsanguineotransfusão imediata (11).
Conforme sua A última atualização de 2022, a AAP também descreve o termo “distúrbio do espectro do kernicterus (DEK)”, proposto para fornecer uma conceituação mais ampla. O DEK abrange todas as sequelas neurológicas da neurotoxicidade da bilirrubina, incluindo os subtipos clássico, motor predominante e auditivo predominante do espectro. Ademais, esta expressão também sugere uma possível associação entre achados sutis de atrasos de desenvolvimento neurológico e concentrações de bilirrubina bem abaixo daquelas associadas ao kernicterus clássico (10).
Por fim, a AAP destaca que a expressão “disfunção neurológica induzida pela bilirrubina” deve ser empregada conforme sua concepção original, isto é, como um escore destinado a quantificar a gravidade da encefalopatia bilirrubínica aguda e o risco de um lactente evoluir subsequentemente para kernicterus ou para a disfunção neurológica crônica induzida pela bilirrubina, devendo-se evitar seu uso para condições nas quais não foi demonstrada relação causal com a bilirrubina (10).
Avaliação clínica e monitorização da bilirrubina
O reconhecimento precoce da etiologia da icterícia é crucial para a prevenção de complicações no curto e longo prazo. O primeiro passo é obter a tipagem sanguínea e a triagem de anticorpos já no pré-natal, seguida por vigilância sistemática para icterícia neonatal após o nascimento, especialmente em RN de alto risco (7). Desde o nascimento até a alta hospitalar, todos os RN devem ser examinados quanto à icterícia e sinais de encefalopatia bilirrubínica aguda pelo menos a cada 12 horas. É importante reconhecer que a icterícia pode não ser tão aparente em RN com tons de pele mais escuros. Além da pele, o médico deve avaliar membranas mucosas e esclera. Quando ocorre nas primeiras 24 horas de vida, deve-se descartar a possibilidade de hemólise. Entretanto, a avaliação visual de forma isolada não deve ser usada para o diagnóstico da icterícia neonatal, sendo necessária a obtenção de valores objetivos de bilirrubina (4).
Investigação laboratorial e métodos avançados (quando disponíveis)
A avaliação clínica da hiperbilirrubinemia patológica é baseada em manifestações clínicas sugestivas de hemólise, avaliação laboratorial (incluindo tipagem sanguínea), teste de antiglobulina direta, índices hematológicos e testes enzimáticos ou genéticos direcionados, com o monóxido de carbono expirado emergindo como um marcador sensível de hemólise. Técnicas avançadas, como a citometria de fluxo e o sequenciamento de nova geração, melhoraram a detecção de condições hemolíticas não identificadas anteriormente, o que possibilita um diagnóstico mais preciso e consequente manejo individualizado. No entanto, é importante considerar, na prática, a disponibilidade, custo e tempo de resposta (7).
Sob luz natural, a digitopressão sobre a pele permite a classificação da icterícia nas zonas de Kramer (zonas dérmicas) (13).
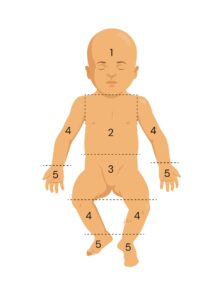 |
Zonas de Kramer | ||
|
Zona |
Local |
Níveis séricos de bilirrubina | |
|
1 |
Cabeça e pescoço |
4 a 8 mg/dL (média 6 mg/dL) | |
|
2 |
Tronco até umbigo |
5 a 12 mg/dL (média 9 mg/dL) | |
|
3 |
Hipogástrio até as coxas |
8 a 17 mg/dL (média 12 mg/dL) | |
|
4 |
Braços, antebraços e pernas |
11 a 18 mg/dL (média 15 mg/dL) | |
|
5 |
Mãos e pés |
>15 mg/dL (média >18 mg/dL) | |
Fonte: Adaptado de Rotinas Assistenciais da Maternidade-Escola da Universidade Federal do Rio de Janeiro.
É importante destacar que a monitorização clínica visual isolada não é suficiente, principalmente em populações de pele preta, devendo ser complementada por métodos objetivos (14). Segundo as diretrizes mais recentes da AAP e da American Academy of Family Physicians (AAFP), a monitorização da bilirrubina consiste em medir a BT sérica ou transcutânea entre 24 e 48 horas após o nascimento ou antes da alta hospitalar. A aferição transcutânea pode ser aplicada como triagem, mas deve ser confirmada por BT sérica se o valor for ≥15 mg/dL ou < 3 mg/dL do limiar para fototerapia (10,15).
Quando repetir BT e como planejar seguimento pós-alta
Caso o RN apresente risco aumentado para icterícia neonatal (como prematuridade, incompatibilidade sanguínea e sinais de hemólise), a monitorização deve ser mais frequente, com repetição da BT em intervalos de 4 a 24 horas conforme o valor inicial e julgamento clínico. Um aumento da BT >0,3 mg/dL/h nas primeiras 24h ou >0,2 mg/dL/h após 24h sugere hemólise e requer atenção especial (4,10,15).
O acompanhamento do RN após alta deve ser feito em 1-2 dias se houver fatores de risco ou alta precoce (<48h), com avaliação clínica e, se necessário, nova medição de BT. Como as concentrações de BT em bebês com icterícia fisiológica atingem o pico entre o terceiro e o quinto dia de vida, período em que a maioria dos bebês costuma já ter recebido alta hospitalar, as mães são, geralmente, as primeiras a observar o início da icterícia grave (8).
Quando indicar fototerapia e outras intervenções?
Para a indicação de fototerapia e transfusão, os níveis séricos de BT não são considerados uniformemente pelos autores. Evidências limitadas levam em conta a dosagem periódica da BT, a idade gestacional (IG) e a idade pós-natal, além das condições agravantes da lesão neuronal pela bilirrubina (2).
Diretriz AAP 2022: limiares por IG e idade pós-natal (≥35 semanas)
Na diretriz da AAP de 2022, constam os seguintes gráficos para RN com IG ≥ 35 semanas:
Limiares de fototerapia por IG e idade em horas para RN sem fatores de risco reconhecidos para neurotoxicidade por hiperbilirrubinemia, além da IG, do nascimento até 72 horas (3 dias);
- Limiares de fototerapia por IG e idade em horas para RN de 3 a 14 dias sem fatores de risco reconhecidos para neurotoxicidade por hiperbilirrubinemia, além da IG;
- Limiares de fototerapia por IG e idade em horas para RN com quaisquer fatores de risco reconhecidos de neurotoxicidade por hiperbilirrubinemia, além da IG, desde o nascimento até 72 horas (ou seja, 3 dias);
- Limiares de fototerapia por IG e idade em horas para RN com quaisquer fatores de risco reconhecidos para neurotoxicidade por hiperbilirrubinemia, além da IG, de 3 a 14 dias;
- Limiares de exsanguineotransfusão por IG para RN sem fatores de risco reconhecidos para neurotoxicidade por hiperbilirrubinemia, além da IG, do nascimento até 72 horas (ou seja, 3 dias);
- Limiares de exsanguineotransfusão por IG para RN sem fatores de risco reconhecidos para neurotoxicidade por hiperbilirrubinemia, além da IG, de 3 a 14 dias;
- Limiares de exsanguineotransfusão por IG para RN com quaisquer fatores de risco reconhecidos para neurotoxicidade por hiperbilirrubinemia, além da IG, do nascimento até 72 horas (ou seja, 3 dias). B, Limiares de exsanguineotransfusão por IG para RN com quaisquer fatores de risco reconhecidos para neurotoxicidade por hiperbilirrubinemia, além da IG, de 3 a 14 dias (10).
Para acesso a estes gráficos, acesse: https://publications.aap.org/pediatrics/article/150/3/e2022058859/188726/Clinical-Practice-Guideline-Revision-Management-of
Valores orientados pela SBP: fototerapia e exsanguineotransfusão
Seguem, abaixo, os valores para fototerapia e exsanguineotransfusão orientados pela Sociedade Brasileira de Pediatria (SBP) (2):
Figura 1: Nível de bilirrubinemia total (mg/dL) para indicação de fototerapia e exsanguineotransfusão em RN ≥35 semanas de idade gestacional ao nascer
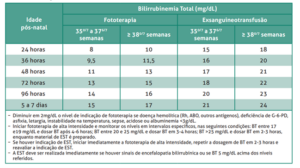
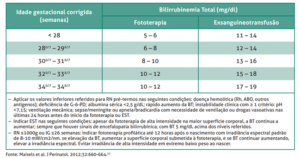
Figura 2: Bilirrubinemia total – BT (mg/dL) para indicação de fototerapia e exsanguineotransfusão em RN <35 semanas de idade gestacional.
Erros comuns no manejo da icterícia neonatal
Os erros mais comuns cometidos durante o manejo da icterícia neonatal consistem em:
- Avaliação inadequada de fatores de risco;
- Confiar somente na inspeção para detectar icterícia, fazendo um diagnóstico visual isolado. Quando há suspeita clínica, a medição objetiva dos níveis de BT sérica ou transcutânea é indispensável.
- Uso inadequado da fototerapia;
- Alta hospitalar precoce sem plano de seguimento;
- Falta de investigação em icterícia prolongada;
- Desconsiderar complicações e sinais de encefalopatia (4,8,10).
Mensagem prática para o pediatra
Na presença de icterícia, o pediatra não deve confiar somente na inspeção. Caso haja dúvidas com relação à zona de Kramer, uma coleta de BT sérica ou a medição transcutânea são obrigatórios. Ao interpretar os gráficos da AAP, é importante que a avaliação seja feita considerando a IG, a idade do RN em horas e a presença ou não de fatores de risco para neurotoxicidade. A ocorrência de kernicterus é totalmente prevenível quando decisões oportunas são tomadas com base em uma avaliação otimizada.
Autoria

Roberta Esteves Vieira de Castro
Graduada em Medicina pela Faculdade de Medicina de Valença ⦁ Residência médica em Pediatria pelo Hospital Federal Cardoso Fontes ⦁ Residência médica em Medicina Intensiva Pediátrica pelo Hospital dos Servidores do Estado do Rio de Janeiro. Mestra em Saúde Materno-Infantil (UFF) ⦁ Doutora em Medicina (UERJ) ⦁ Aperfeiçoamento em neurointensivismo (IDOR) ⦁ Médica da Unidade de Terapia Intensiva Pediátrica (UTIP) do Hospital Universitário Pedro Ernesto (HUPE) da UERJ ⦁ Professora adjunta de pediatria do curso de Medicina da Fundação Técnico-Educacional Souza Marques ⦁ Membro da Rede Brasileira de Pesquisa em Pediatria do IDOR no Rio de Janeiro ⦁ Acompanhou as UTI Pediátrica e Cardíaca do Hospital for Sick Children (Sick Kids) em Toronto, Canadá, supervisionada pelo Dr. Peter Cox ⦁ Membro da Sociedade Brasileira de Pediatria (SBP) e da Associação de Medicina Intensiva Brasileira (AMIB) ⦁ Membro do comitê de sedação, analgesia e delirium da AMIB e da Sociedade Latino-Americana de Cuidados Intensivos Pediátricos (SLACIP) ⦁ Membro da diretoria da American Delirium Society (ADS) ⦁ Coordenadora e cofundadora do Latin American Delirium Special Interest Group (LADIG) ⦁ Membro de apoio da Society for Pediatric Sedation (SPS) ⦁ Consultora de sono infantil e de amamentação ⦁ Instagram: @draroberta_pediatra
Como você avalia este conteúdo?
Sua opinião ajudará outros médicos a encontrar conteúdos mais relevantes.

