A Agência Nacional de Vigilância Sanitária (Anvisa) decidiu em reunião extraordinária nesta terça-feira (22) a liberação do uso das vacinas bivalentes Comirnaty Bivalente BA.1 e Comirnaty Bivalente BA.4/BA.5, ambas da Pfizer.
Diante da situação epidemiológica atual do país, as doses vão servir para proteger a população contra a cepa original, a Ômicron e as demais variantes.
No Brasil, os casos de covid-19 aumentaram nos últimos meses com subvariantes da variante Ômicron em circulação. A aplicação do imunizante é indicada apenas para maiores de 12 anos.
Leia também: Anvisa aprova remdesivir para pacientes pediátricos com covid-19
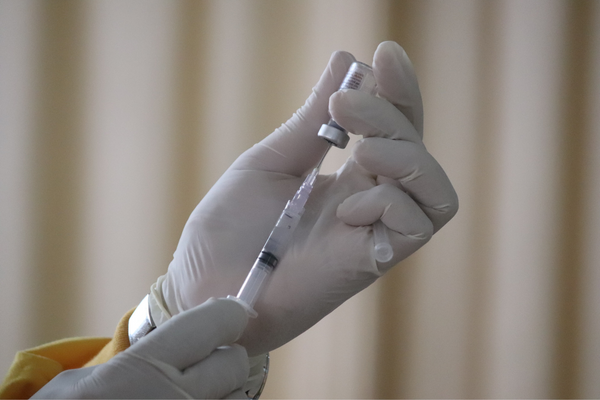
Benefícios identificados
Segundo a conclusão da Agência, os benefícios conhecidos e potenciais das vacinas superam os riscos conhecidos e potenciais para a prevenção da doença, quando administradas como dose de reforço pelo menos três meses após a vacinação primária ou recebimento da dose de reforço mais recente, com qualquer vacina covid-19 monovalente aprovada.
O pedido de uso emergencial das vacinas bivalentes foi enviado pela Pfizer à Anvisa no dia 30 de setembro.
Aumento de casos de covid-19 pelo mundo
A nova subvariante BQ.1 tem provocado aumento de casos na Europa desde meados do ano.
Autoria

Redação Afya
Produção realizada por jornalistas da Afya, em colaboração com a equipe de editores médicos.
Como você avalia este conteúdo?
Sua opinião ajudará outros médicos a encontrar conteúdos mais relevantes.

