Paciente do sexo masculino, 72 anos, procurou atendimento por dispneia progressiva até esforços habituais (classe funcional II) com evolução em 6 meses, acompanhado de edema em membros inferiores. Referia também tontura com turvação visual ao mudar da posição sentada para ortostática. Negava dor torácica e síncope. Tinha como antecedentes hipertensão arterial sistêmica controlada com losartana 50mg 1x ao dia e síndrome do túnel do carpo em seguimento clínico. Exame clínico inicial mostrava pressão arterial (PA) 122×80 deitado e 90×62 em pé, frequência cardíaca (FC) 90bpm, presença de turgência jugular, ausculta pulmonar com estertores crepitantes em bases e cardíaca sem alterações, abdome flácido, indolor, extremidades com edema +/4+. Solicitados exames para avaliação inicial. Laboratório com NT- proBNP de 8452 pg/mL, sem outras alterações relevantes.
Eletrocardiograma (ECG)
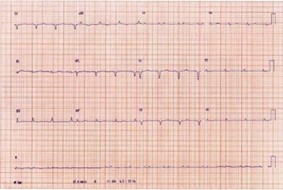
Ecocardiograma transtorácico (ecoTT) com fração de ejeção do ventrículo esquerdo (FEVE) 64%, átrio esquerdo levemente aumentado, diâmetros do ventrículo esquerdo (VE) de tamanho normal, septo 12mm, parede posterior do VE 12mm, hipertrofia concêntrica leve, índice de massa aumentado, sem alteração segmentar e sem alteração valvar, disfunção diastólica grau II e derrame pericárdico discreto.
A losartana foi suspensa e foi iniciada furosemida com melhora do edema dos membros inferiores e da dispneia, que passou a ocorrer apenas após grandes esforços (classe funcional I). O paciente recebeu alta para seguimento ambulatorial.
Como o paciente apresentava ondas Q no eletrocardiograma e o ecoTT não mostrou alteração segmentar, optou-se pela realização de ressonância miocárdica (RM) que mostrou VE com realce tardio subendocárdico circunferencial e padrão sugestivo de amiloidose cardíaca.
Foram realizados exames de imunofixação e eletroforese de proteínas séricas e urinárias que não mostraram pico monoclonal. O paciente foi então submetido a exame de cintilografia com pirofosfato, que mostrou achado compatível com amiloidose cardíaca. Feito diagnóstico de amiloidose ATTR, foi solicitada avaliação genética e o paciente iniciou tratamento com tafamidis 80mg 1x ao dia.
No seguimento mantinha dispneia apenas aos grandes esforços, sem outras queixas, sem necessidade de novas internações.
Discussão
Atualmente, o paciente com insuficiência cardíaca (IC) é classificado como tendo IC com fração de ejeção reduzida (ICFER), quando a fração de ejeção do ventrículo esquerdo (FEVE) é ≤ 40%, ou com fração de ejeção preservada (ICFEP), quando a FEVE é ≥ 50%. Essa classificação é importante pois o prognóstico e a resposta ao tratamento são diferentes. Quando a FEVE está entre 40 e 50%, denominamos a IC como sendo levemente reduzida.1
O diagnóstico de ICFEP pode ser desafiador, pois exige a presença de sintomas e alterações estruturais e/ou funcionais do coração. Essas alterações são representadas pelo aumento das pressões de enchimento ao repouso ou ao esforço, avaliados por exames de imagem e por aumento do peptídeo natriurético cerebral (BNP) ou o fragmento inativo do mesmo pró‑hormônio (NT-proBNP).1,2
Alguns escores facilitam o diagnóstico. O H2FPEF, por exemplo, leva em conta as seguintes variáveis: obesidade (heavy), uso de pelo menos 2 anti-hipertensivos (hipertensão), fibrilação atrial (FA), pressão sistólica da artéria pulmonar (PSAP) > 35mmHg, idade (elderly) > 60 anos, ecocardiograma com relação E/e’ > 9 (Filling pressure). A probabilidade de IC é baixa quando o escore é < 2 e alta quando ≥ 6.1,3
A ICFEP é altamente prevalente, correspondendo a até 50% dos casos de IC. Apresenta morbimortalidade importante e esses pacientes costumam ter comorbidades como hipertensão, diabetes, obesidade, doença arterial coronariana (DAC) e doença renal crônica (DRC). Porém, uma parte deles pode ter também outras doenças específicas do coração, como a amiloidose.1,4
As causas da IC devem sempre ser investigadas, pois pode existir tratamento específico direcionado. A avaliação laboratorial inicial inclui hemograma, função renal e eletrólitos, glicose, perfil lipídico, função hepática, perfil de ferro, hormônios da tireoide e ECG. O ecoTT é o exame de imagem de escolha inicial e dá informações diagnósticas e prognósticas, além de classificar o paciente em ICFER e ICFEP, que, como já comentado, muda o tratamento.1
Uma causa cada vez mais reconhecida de IC é a amiloidose cardíaca, causada por depósito de proteína amiloide no espaço extracelular. As mais frequentes são a amiloidose por deposição da cadeia leve de imunoglobulina (AL) e a amiloidose por transtirretina (ATTR).1
A AL é considerada doença hematológica, tratada sistemicamente pelo hematologista. Já a ATTR é doença tratada pelo cardiologista, sendo extremamente importante diferenciá-las.1
A transtirretina (TTR) é uma proteína produzida pelo fígado, constituída por um tetrâmero. Quando há alteração no seu gene, ocorre dissociação das suas subunidades e formação de fibrilas anormais, que se agregam e depositam em diversos órgãos. O coração é um dos principais afetados, e seu acometimento está associado a baixa expectativa de vida, geralmente de 2 a 6 anos após o diagnóstico.5,6
A ATTR pode ser herdada, causada por diversas variantes genéticas e chamada ATTRv, ou pode ser causada por uma nova mutação, ou forma selvagem (do inglês wild-type), chamada ATTRwt.6
A ATTR ocorre mais em homens e idosos.5,7 Estudos de autópsia mostraram que 25% dos idosos com mais de 80 anos tinham alteração compatível com amiloidose.5 A idade média ao diagnóstico é entre 74 e 90 anos e as mulheres costumam manifestar 3 anos mais tarde que os homens.8,9,10
A forma ATTRwt é a mais comum (75% dos casos), se manifesta mais frequentemente com cardiomiopatia e menos de 10% dos pacientes tem polineuropatia concomitante.5 A prevalência da forma ATTRv é estimada em 40 a 50 mil pessoas no mundo,6 geralmente transmitida de forma autossômica dominante e tem penetrância variável.5 As manifestações clínicas da ATTRv podem ser cardíacas, neurológicas ou ambas.6
A deposição da proteína amiloide no espaço intersticial, entre os miócitos, contribui para a disfunção miocárdica, espessamento ventricular progressivo e alteração da função sistólica longitudinal. Ocorre injúria miocelular, manifesta como aumento de troponina.5
A evolução ocorre ao longo de anos ou até mesmo décadas e a principal manifestação é a IC, tipicamente ICFEP no início, porém também pode haver alterações do sistema de condução e arritmias como FA ou taquicardia ventricular.5 Os sintomas mais frequentes são dispneia, ortopneia, dispneia paroxística noturna, intolerância aos esforços, fadiga, capacidade funcional reduzida e edema, mas também podem ocorrer tontura, palpitação, sintomas de neuropatia sensitivo-motora e gastrointestinais.5,6
Como frequentemente os pacientes são idosos e apresentam outras comorbidades que podem muitas vezes justificar os sintomas e aumento da espessura do VE, o diagnóstico acaba não sendo realizado ou é tardio.5,6 Assim, para diagnosticar corretamente deve-se ter alta suspeita, geralmente levantada quando há ocorrência de sintomas de IC na presença de discordância entre a espessura da parede do VE ou sua massa no ecoTT e a voltagem no ECG, achado bastante característico.1,6,12
A baixa voltagem no ECG ocorre em 50% das amiloidoses AL e 25% das ATTR e, como comentado, geralmente é desproporcional à espessura do VE no ecoTT. Outras alterações encontradas são o padrão de pseudoinfarto com ondas Q não relacionadas a infarto prévio, FA, bloqueios atrioventriculares ou arritmias ventriculares.1,5,6
A doença também deve ser suspeitada em casos de idosos com IC, fenótipo hipertrófico no ecoTT e níveis de troponina ou peptídeos natriuréticos aumentados de forma desproporcional ao contexto clínico ou ainda quando há hipertensão que se resolve com o tempo ou intolerância a vasodilatadores, como inibidores da enzima conversora de angiotensina (IECA), bloqueadores do receptor de angiotensina (BRA) ou intolerância aos betabloqueadores (BB).5,6
Outros red flags não relacionados ao sistema cardiovascular são a ocorrência de síndrome do túnel do carpo, estenose de canal medular e ruptura espontânea de ligamentos, como do tendão do bíceps, decorrentes de depósito amiloide nesses locais.5, 6,12 Além disso, uma parte dos pacientes com estenose aórtica importante também tem amiloidose.1
O ecoTT é custo efetivo, disponível, rápido e consegue avaliar a disfunção diastólica. Os achados clássicos são aumento da espessura da parede do VE, cavidade de tamanho pequeno, aumento biatrial, espessamento valvar, aumento da espessura do septo atrial e aparência granular na parede do miocárdio, além de derrame pericárdico, padrão restritivo ao doppler e redução do strain ventricular. 6
A RM pode auxiliar, já que mostra informações detalhadas de função sistólica e estrutura do coração, além de permitir a caracterização tecidual. É um exame muito útil para excluir a doença, mas não consegue estabelecer o diagnóstico isoladamente ou diferenciar entre as formas AL e ATTR.13,14 Os achados típicos são realce tardio difuso pelo gadolínio, regiões de realce subendocárdico e transmural distintas de outras alterações cardíacas e volume extracelular aumentado para valores maiores que 40%.1,5,6
O exame de imagem mais específico é a cintilografia com tecnécio e marcadores específicos.1 Assim, para o diagnóstico da amiloidose ATTR deve-se primeiro excluir a presença de picos monoclonais de cadeia leve, com pesquisa de proteínas de cadeias leves no sangue e eletroforese de proteínas séricas e urinárias. Com esses exames negativos, indica-se a realização de cintilografia com pirofosfato, ácido 3,3 difosfono-1,2 propanodicarboxílico ou hidrometileno-difosfonato. O pirofosfato é um dos marcadores mais utilizados e quando há captação grau 2/3 no coração, na ausência da presença de picos monoclonais, considera-se exame bastante específico para ATTR, com valor preditivo positivo próximo de 100%, sendo isto suficiente para o diagnóstico.1,5,15
Confirmada a doença, realiza-se o sequenciamento genético para determinar o tipo, ATTRv ou ATTRwt, no intuito de guiar a investigação de familiares.1 (Figura 1)
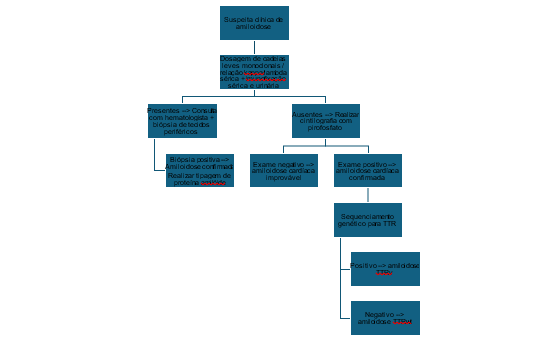
Figura 1 – Fluxograma para diagnóstico de amiloidose cardíaca
A biópsia endomiocárdica, que mostra depósito de fibrilas amiloides na coloração vermelho congo é o padrão-ouro. Porém, é reservada para casos com alta suspeita clínica de amiloidose ATTR em pacientes com pico monoclonal concomitante, alta suspeita clínica apesar de cintilografia negativa ou cintilografia indisponível.11
O tratamento é o habitual para ICFEP, com diuréticos para alívio de congestão e sintomas, manejo das comorbidades relacionadas e o tratamento específico para amiloidose.1
O diurético de escolha é o de alça, porém antagonistas mineralocorticoides podem contribuir para aumentar a diurese e auxiliar na redução da hipocalemia. Caso a resposta seja ruim pode-se associar tiazídicos.5 Os inibidores de SGLT2 estão indicados na ICFEP com objetivo de reduzir mortalidade e internações hospitalares, porém não há estudos específicos na amiloidose.1
O controle dos fatores de risco como hipertensão, DAC e FA deve ser sempre realizado, porém pacientes com amiloidose costumam ter baixa tolerância a vasodilatadores e BB, por conta de disfunção autonômica.1 Assim, a avaliação de hipotensão ortostática é importante para reduzir os riscos associados às medicações, que podem desencadear hipotensão sintomática e síncope.5
O tratamento específico é feito com medicações que se ligam e estabilizam a proteína TTR, inibindo a dissociação do tetrâmero e diminuindo a formação de amiloide. Uma das medicações aprovadas atualmente para amiloidose cardíaca é o tafamidis, que foi avaliado em um estudo que testou a dose de tafamidis 20mg ou 80mg 1x ao dia comparado ao placebo por 30 meses em pacientes com classe funcional (CF) da New York Heart Association (NYHA) I a III. Houve redução significativa de mortalidade (29,5% x 42,9%) e internações por IC com número necessário para tratar (NNT) 7 ou 8 para prevenir 1 morte e NNT 4 para prevenir 1 internação.16
Um estudo publicado em 2020 testou o tafamidis em sua forma de ácido livre, na dose de 61mg, comparado ao tafamidis meglumina na dose de 80mg e mostrou eficácia semelhante entre as duas formas da medicação, sendo ambas indicadas para o tratamento da doença.17
O tafamidis diminui a progressão da doença, mas não necessariamente a faz regredir, já que não reverte o depósito amiloide já existente, sendo mais eficaz em estágios mais precoces da doença (CF I ou II).11 Também melhora capacidade funcional e qualidade de vida.16 Não parece haver benefício quando se está em CF IV, estenose aórtica importante e disfunção renal avançada.1
Assim, deve ser indicado se houver benefício potencial significativo, ou seja, doença clinicamente relevante e ausência de outras comorbidades que reduzam a sobrevida.11
Ponto importante é em relação a FA e anticoagulação, que está indicada independente do CHA2DS2-VASc, pois o risco de evento tromboembólico desses pacientes é aumentado.18,19
Existem outras medicações que suprimem a produção hepática de TTR, porém estas foram testadas para os pacientes com polineuropatia, não sendo atualmente recomendadas para pacientes com cardiomiopatia isolada.5
Conclusão
Amiloidose é causa subdiagnosticada de IC, principalmente ICFEP, mas deve sempre ser suspeita quando existir história de IC, presença de um ou mais red flags ou exames complementares com características suspeitas. Esses pacientes têm risco de evolução desfavorável e atualmente há medicação específica possível de ser utilizada com grande benefício, inclusive em mortalidade. A medicação já foi incorporada pelo Sistema Único de Saúde (SUS) e o tafamidis na dose de 61mg pode ser utilizado sem custo para os pacientes desde a publicação da Portaria SECTICS/MS no 26, de 19 de junho de 2024.
PP-VDMBRA-0121
Copyright © 2026 Grupo Pfizer. Todos os direitos reservados. Material de distribuição exclusiva a profissionais de saúde habilitados a prescrever ou dispensar medicamentos. Proibida a reprodução ou compartilhamento com terceiros.
Acesse aqui a bula completa de Vyndaqel®
INTERAÇÃO MEDICAMENTOSA MAIS FREQUENTE: O tafamidis tem o potencial de inibir o transportador de efluxo BCRP (proteína resistente ao câncer de mama) e de aumentar a exposição sistêmica dos substratos deste transportador, o que pode causar interações medicamentosas com os mesmos (por exemplo, metotrexato, rosuvastatina, atorvastatina, apixabana, rivaroxabana e imatinibe). O tafamidis pode ter o potencial de inibir os transportadores de ânions orgânicos 1 (OAT1) e pode causar interações fármaco-fármaco com substratos deste transportador (p. ex., medicamentos anti-inflamatórios não esteroides, bumetanida, furosemida, lamivudina, metotrexato, oseltamivir, tenofovir, ganciclovir, adefovir, cidofovir, zidovudina,
zalcitabina). Entretanto, não é esperado que a inibição dos transportadores OAT1 por tafamidis resulte em interações clinicamente significativas. O tafamidis não inibe o transportador de ânions orgânicos 3 (OAT3).
CONTRAINDICAÇÃO MAIS FREQUENTE: VYNKELLA® É CONTRAINDICADO A PACIENTES COM HIPERSENSIBILIDADE CONHECIDA AO TAFAMIDIS OU A QUALQUER OUTRO COMPONENTE DA FÓRMULA.
Autoria

Isabela Abud Manta
Editora médica de Cardiologia da Afya ⦁ Residência em Clínica Médica pela UNIFESP ⦁ Residência em Cardiologia pelo Instituto do Coração (InCor) do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo (USP) ⦁ Graduação em Medicina pela Escola Paulista de Medicina da Universidade Federal de São Paulo (UNIFESP) ⦁ Atua nas áreas de terapia intensiva, cardiologia ambulatorial, enfermaria e em ensino médico.
Como você avalia este conteúdo?
Sua opinião ajudará outros médicos a encontrar conteúdos mais relevantes.



