Na última quarta-feira, 07, a European Medicines Agency (EMA) emitiu uma nota confirmando a potencial relação entre a vacina contra a Covid-19 desenvolvida pela Universidade de Oxford e a farmacêutica AstraZeneca com ocorrências de trombose com trombocitopenia.
Apesar disso, a agência reforçou que o risco é baixíssimo e recomendou a continuidade da vacinação, o que foi apoiado por outros órgãos, como a Organização Mundial da Saúde (OMS) e a própria Agência Nacional de Vigilância Sanitária (Anvisa).
Segundo os dados divulgados pela EMA, foram cerca de seis casos a cada 1 milhão de vacinados (0,0006%) no Espaço Econômico Europeu e no Reino Unido, onde mais de 34 milhões de pessoas receberam a vacina, portanto os benefícios superam os riscos. No Brasil, entre os 4 milhões de vacinados, 47 casos suspeitos estão sendo avaliados, sendo apenas um deles associado à trombocitopenia.
A Anvisa solicitou à farmacêutica inclua a informação de possíveis eventos tromboembólicos na parte de advertências e precauções da bula da vacina, mas deixou claro que os casos são raríssimos e ainda são necessários mais estudos para confirmar que os casos estão relacionados à vacina.
Leia também: Vacina de Oxford será testada em crianças e adolescentes pela primeira vez
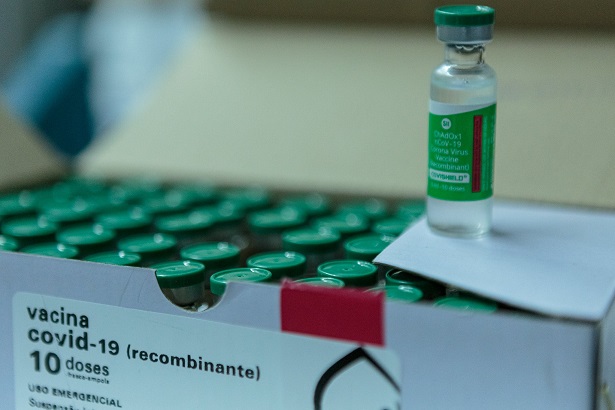
Vacina de Oxford e trombose
Até agora, a maioria dos casos relatados na Europa ocorreu em mulheres com menos de 60 anos de idade nas duas semanas seguintes à imunização. O comitê de segurança da EMA relatou que os casos mais comuns foram de trombose venosa cerebral e trombose da veia esplênica.
Os médicos e profissionais de saúde devem alertar os pacientes a procurarem atendimento em caso de falta de ar, dor no peito, inchaço na perna, dor abdominal persistente, sintomas neurológicos, incluindo dores de cabeça persistentes ou visão turva, ou pequenas manchas de sangue sob a pele em até duas semanas após a aplicação.
Apesar de a agência europeia ter relacionado os casos às mulheres jovens, a Anvisa ressaltou que ainda não foram identificados os fatores de risco específicos para o evento.
Notificação
Os profissionais de saúde devem informar sempre que identificarem um possível efeito adverso das vacinas. A notificação deve seguir o fluxo estabelecido pelo Protocolo de Vigilância Epidemiológica e Sanitária de Eventos Adversos Pós Vacinação.
A sinalização pode ser feita pelo e-SUS Notifica, ou pelo formulário do VigiMed para profissionais sem vínculo institucional.
Para problemas de qualidade ou queixas técnicas de produtos utilizados na vacinação, é necessário utilizar o Sistema de Notificações em Vigilância Sanitária – Notivisa.
*Esse artigo foi revisado pela equipe médica da PEBMED
Referências bibliográficas:
- AstraZeneca’s COVID-19 vaccine: EMA finds possible link to very rare cases of unusual blood clots with low blood platelets. European Medicines Agency. 07 Apr 2021. https://www.ema.europa.eu/en/news/astrazenecas-covid-19-vaccine-ema-finds-possible-link-very-rare-cases-unusual-blood-clots-low-blood
- Anvisa solicita . Portal Anvisa. 07 de abril de 2021. https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2021/anvisa-solicita-alteracao-de-bula-da-vacina-de-oxford
- Alteração de bula da vacina de Oxford/AtraZeneca/Fiocruz contra a Covid-19. Comunicado GGMON 004/2021. Vacinas Contra a Covid-19. 07 de abril de 2021. https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2021/anvisa-solicita-alteracao-de-bula-da-vacina-de-oxford/comunicado_ggmon_004_2021.pdf
Autoria

Clara Barreto
Jornalista formada pela Universidade Federal Fluminense (UFF) ⦁ Especialista em Divulgação Científica e Popularização da Ciência pela Fundação Oswaldo Cruz (Fiocruz).
Como você avalia este conteúdo?
Sua opinião ajudará outros médicos a encontrar conteúdos mais relevantes.

